Zielgerichtete Krebstherapie bei Hunden erforscht
Auch Hunde leiden an Krebserkrankungen, wie wir Menschen. WissenschafterInnen an der Veterinärmedizinischen Universität Wien erforschen nun die molekularen Prozesse der Krebsentwicklung an Hundezellen. Denn die moderne Krebstherapie wurde mit der Einführung neuer Medikamente, sogenannter gezielter Wirkstoffe, revolutioniert. Die Grundlagen für eine erfolgreiche Anwendung dieser neuen Wirkstoffe in der Krebstherapie erfordert jedoch ein tieferes Verständnis der molekularen Vorgänge der Erkrankung auch bei Haustieren. Jetzt hat ein Forschungsteam um Sabine Macho-Maschler die Aktivierung von genetischen Regulationsmechanismen an Hundezellen untersucht und sowohl Übereinstimmungen als auch Unterschiede im Vergleich zum Menschen gefunden.
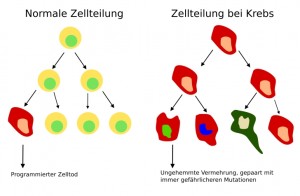
Fast jeder zweite Hund im Alter von zehn Jahren entwickelt eine Krebserkrankung. Eine moderne Tumortherapie verbindet Chirurgie, Strahlentherapie und neue medikamentöse Behandlungsmöglichkeiten. Während bei Chirurgie und Strahlentherapie eine adäquate Behandlung für alle Tiere an der Vetmeduni Vienna gewährleistet ist, klafft bei der Behandlung mit neuen gezielten Wirkstoffen zunehmend eine Lücke. Der Grund dafür ist, dass moderne Behandlungen auf konkreten molekulargenetischen Befunden beruhen, die vom Menschen oder dem bevorzugten Tiermodell der Krebsforschung, der Maus, nicht einfach auf Hunde zu übertragen sind. Es bedarf also einer vergleichenden Erforschung der molekularen Grundlagen von Krebs beim Hund, um moderne Krebsmedikamente auch für unsere vierbeinigen Freunde zugänglich zu machen.
Molekulare Ursachen stellen eine wichtige Grundlage für moderne Behandlungskonzepte dar
Das Verständnis der molekularen und zellulären Ursachen, die für die Krebsentstehung verantwortlich sind, ist in den letzten Jahren stark gewachsen. Dieses Wissen hilft, Krebszellen gezielt mit einer wachsenden Anzahl neuer Medikamente zu bekämpfen. Da Krebs aber in jeder Patientin bzw. in jedem Patienten individuelle Veränderungen aufweisen kann, ist eine aufwendige molekulare Untersuchung der tatsächlich vorliegenden Mutationen in Krebszellen eine wichtige Voraussetzung. Denn die gezielten Wirkstoffe können nur dann helfen, wenn die Krebszellen auch die entsprechenden molekularen Strukturen aufweisen, gegen die das Medikament wirken soll. Der Behandlungserfolg gezielter Wirkstoffe setzt also eine molekulare Diagnostik voraus, die als Grundlage für die sogenannte personalisierte Medizin in der Krebsforschung gilt.
Molekulare Mechanismen der Metastasierung bei Hundezellen untersucht
Ein Forschungsteam an der Abteilung für Molekulare Genetik hat jetzt einen wichtigen Prozess in der Krebsentstehung molekulargenetisch an einer Zelllinie von Hunden untersucht. An dieser Zelllinie, die schon seit vielen Jahren von WissenschafterInnen verwendet wird, auch um pathologische Prozesse zu erforschen, wurde nun eine differentielle Analyse der Genexpression während der epithelial-mesenchymalen Transition (EMT) durchgeführt. EMT, also die Umwandlung von Epithelzellen zu mesenchymalen Zellen, wird mit der Möglichkeit der Metastasierung von Krebszellen in Verbindung gebracht. An den „Campus Science Support Facilities, (CSF)“ in Wien (Link zur Website), welche über die relevante Expertise und instrumentelle Ausrüstung verfügen, wurde mit modernen Sequenzierungsmethoden („Next Generation Sequencing“) die Expression von verschiedenen RNA-Formen in den Zellen vor und nach der EMT bestimmt. „Krebsforschende arbeiten schon viele Jahre an dem Übergang epithelialer Tumorzellen in einen aggressiveren mesenchymalen Zustand. Dabei konnten wichtige Genschalter identifiziert werden, die sich auch als therapeutische Zielstrukturen eignen: also Genprodukte, die man mittels gezielter Wirkstoffe ausschalten könnte“, erklärt Macho-Maschler, die die jetzt publizierte Studie leitete. Die Forschung am Übergang von epithelialen zu mesenchymalen Zellen fand bislang hauptsächlich an Zellen von Mäusen und Menschen statt und hat gezeigt, wie bestimmte Signalübertragungswege kooperieren, um Krebszellen die Metastasierung zu ermöglichen. Metastasen bilden sich, wenn die ursprünglich sesshaften Krebszellen bestimmte Eigenschaften erhalten, die es ihnen erlauben in ein anderes Organ zu wandern und dort eine neue Geschwulst zu bilden. „Es sind in den überwiegenden Fällen die Metastasen, die PatientInnen das Leben kosten, denn der ursprüngliche Tumor lässt sich durch Bestrahlung und Operation oft gut kontrollieren“, betont Mathias Müller, Leiter des Instituts für Tierzucht und Genetik. „Es interessiert uns, was auf molekularer Ebene während der Metastasierung in den Zellen vorgeht, weil wir dieses Wissen möglicherweise für eine erfolgreiche Behandlung dieser Metastasen verwenden können.“
Basis für weitere Forschung gelegt
Die molekulare Analyse der EMT wird von den Forschenden als Modell für den Erwerb der Fähigkeit zur Metastasierung betrachtet. Der TGF-beta Signalweg ist schon lange als zentraler Schalter in der EMT bekannt. Macho-Maschler zeigt sich zufrieden über die vielen Ähnlichkeiten bei der vergleichenden Analyse von Ergebnissen für Hunde, Menschen und Mauszellen. „TGF-beta spielt beispielsweise auch beim Hund eine wichtige Rolle, aber es gibt interessante Abweichungen“, weiß sie zu berichten. Ihre zuletzt in BMC Genomics erschienene Veröffentlichung ist voller langer Listen von RNAs, die während der EMT reguliert sind. Diese Forschungsergebnisse sollen als Grundlage für weiterführende Analysen dienen. Macho-Maschler äußert sich kritisch, ob ihre Forschung schon bald die Behandlung von Hunden mit Krebs verbessern kann. „Unsere jetzt publizierten Ergebnisse sind wie ein Katalog, vielleicht eine wichtige Voraussetzung für neue Ansätze und Ideen. Letztlich wissen wir bei vielen der neuen Krebsmedikamente noch nicht einmal, ob sie bei Hundezellen tatsächlich wirken. Es gibt beispielsweise auch Wirkstoffe, die nur beim Menschen, aber nicht bei der Maus wirken“, dämpft sie zu hohe Erwartungen. Beim Menschen wurde ein ungleich umfangreicherer Katalog dieses Jahr fertiggestellt. „The Cancer Genome Atlas (TCGA)“ enthält mit über 11.000 genetisch analysierten PatientInnenproben Informationen, die für alle Forschenden zugänglich sind. Der TCGA ist eine wichtige Ressource, beispielsweise um die Häufigkeit bestimmter genetischer Veränderungen in einer Krebsart schnell und zuverlässig zu erheben. Der Katalog von Macho-Maschler ist mit dem TCGA natürlich nicht zu vergleichen, aber es ist ein erster kleiner Schritt in die gleiche Richtung für Hundekrebs.
